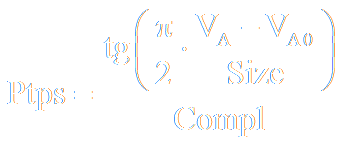Idea projektu
 Istnieje szereg modeli układu oddechowego (UO), ale zazwyczaj co najmniej jeden rodzaj zjawisk fizjologicznych albo jest brany pod uwagę w dużym uproszczeniu albo w ogóle jest ignorowany. Na przykład następujące aspekty są często pomijane:
Istnieje szereg modeli układu oddechowego (UO), ale zazwyczaj co najmniej jeden rodzaj zjawisk fizjologicznych albo jest brany pod uwagę w dużym uproszczeniu albo w ogóle jest ignorowany. Na przykład następujące aspekty są często pomijane:
- wpływ grawitacji i innych czynników na rozkład wentylacji i perfuzji,
- taki opis matematyczny oskrzeli, który umożliwia poprawną symulację przepływu powietrza podczas zarówno spokojnych wdechów i wydechów jak i forsownych (jak podczas spirometrii) oraz wszystkich pośrednich sposobów oddychania, tak w przypadku zdrowego UO jak i jego chorób,
- układ o stałych rozłożonych transferu gazów w drogach oddechowych oraz transportu z krwią, wymiana gazowa w płucach i konsumpcja tlenu w tkankach, buforowanie CO2,
- znaczące nieliniowości w krążeniu płucnym i zależność jego parametrów od wielu parametrów takich jak, na przykład, okołonaczyniowa prężność tlenu, etc.
Oczywiście prosty model może być użyteczny w konkretnym jednostkowym zastosowaniu zdefiniowanym przed budową modelu. Jednakże jeśli jakiś model ma być używany w zastosowaniach niezdefiniowanych przed budową tego modelu, musi on uwzględniać tak wiele czynników i zjawisk, jak to możliwe. Na przykład, jeśli model ma służyć innym naukowcom lub w edukacji lub do testowania nowej aparatury, musi on tak wiernie odzwierciedlać rzeczywistość jak to tylko możliwe. Bo, rzeczywiście, nie możemy znać przyszłych prac innych naukowców, nie możemy przewidzieć radosnej inwencji studentów, zazwyczaj nie możemy znać a priori wszystkich cech UO, które są istotne w przypadku nowego urządzenia (e.g. Golczewski T, Palko KJ. Biocybern Biomed Eng 2013; 33:136-144).
Autorzy modeli układu krążenia, tj. serca i krążenia systemowego, zazwyczaj wykorzystują skrajnie proste modele UO aby dostarczyć swojemu modelowi krążenia wartości ciśnień i przepływów płucnych oraz saturacji. Może to być związane z faktem, że specjaliści od układu krążenia często nie są specjalistami od fizjologii płuc.
Nasz wirtualny pacjent pneumonologiczny jako biała skrzynka.
Biorąc powyższe pod uwagę, celem projektu jest przygotowanie naszego modelu jako tzw. białej skrzynki dostępnej dla wszystkich poprzez Internet aby umożliwić innym naukowcom i wykładowcom jej wykorzystanie jako dodatek do swoich modeli lub jako samodzielny model w ich badaniach lub edukacji.
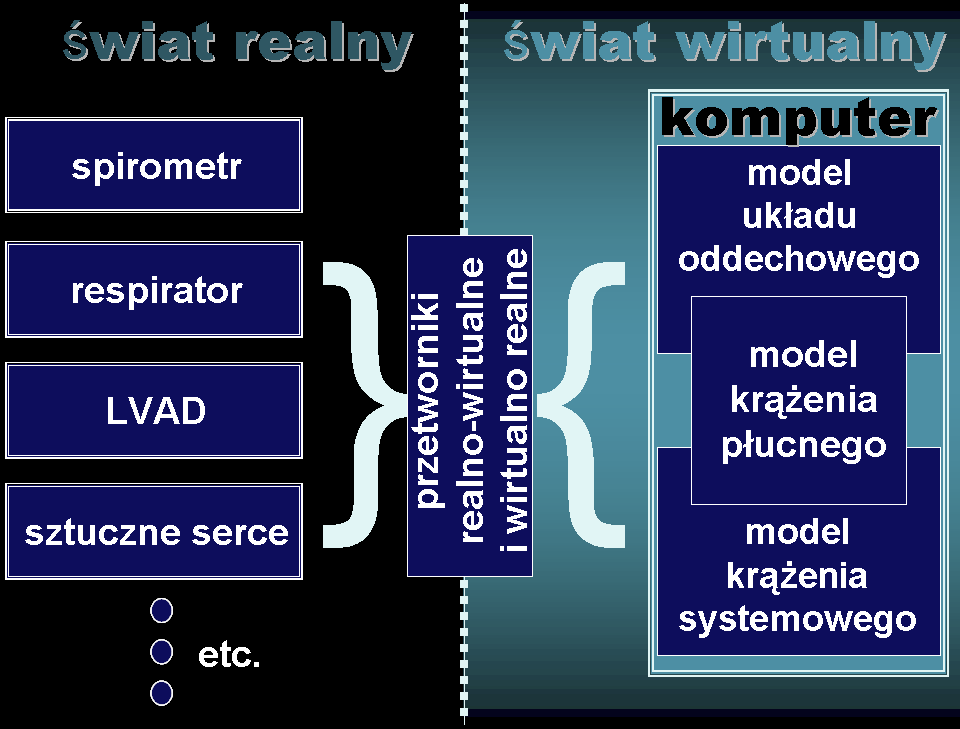
Ta biała skrzynka ma trzy wejścia i trzy wyjścia, jak pokazano na rysunku. Parametry oddechu (czasy wdechu i wydechu, objętość oddechowa) mogą być podane ręcznie lub jako funkcja prężności tlenu i dwutlenku węgla we krwi tętniczej. Wartości fizjologicznie interpretowalnych parametrów UO mogą być zmieniane jako procenty pewnych wartości standardowych. Jeśli użytkownik nie ma własnego układu krążenia systemowego, prosty model tego układy dostarczy danych będących wejściem białej skrzynki.
Sztuczny pacjent oddechowo-krążeniowy
Nasz sztuczny pacjent oddechowo-krążeniowy jest zbiorem wzajemnie ze sobą współpracujących modeli, który może kontaktować się ze światem zewnętrznym, np. medyczną aparaturą diagnostyczną lub terapeutyczną, za pomocą naszych przetworników realno-wirtualnych. W zależności od konkretnego zastosowania, część komputerowa składa się z jednego lub z kilku współpracujących ze sobą następujących modeli:
- model mechaniki układu oddechowego,
- model krążenia płucnego,
- model krążenia systemowego (we współpracy z Istituto di Fisiologia Clinica, Włochy),
- model transferu gazów i wymiany gazowej składający się z modułów: transferu gazów w układzie oddechowym, wymiany gazowej w płucach, transportu gazów z krwią w krążeniu płucnym oraz transportu oraz takiego transportu w krążeniu systemowym,
- dodatkowe modele fizjologii takie jak modele: sterowania oddechem na podstawie prężności gazów we krwi tętniczej, odruchu z baroreceptorów (we współpracy z Istituto di Fisiologia Clinica, Włochy), itp.,
- modele aparatury medycznej jeśli wstępne badania nie wymagają testowania realnego sprzętu.
Wybrane szczegóły modeli
Elementy o stałych rozłożonych
Rury, które są zarówno znacząco podatne jak i znacząco oporowe, tak jak płucne kapilary i oskrzela średniego rzędu, muszą być reprezentowane przez modele o stałych rozłożonych. Rzeczywiście, jeśli płyn płynie wzdłuż takiej rury, to ciśnienie transmuralne determinujące przekrój rury (skoro rura jest podatna) maleje wzdłuż tej rury (skoro rura jest oporowa). A więc przekrój maleje wzdłuż rury zwiększając lokalny opór, co zwiększa spadek ciśnienia, co zmniejsza przekrój, itd.
Z drugiej jednak strony, symulacje za pomocą modeli o stałych rozłożonych są bardzo czasochłonne, podczas gdy sztuczny pacjent musi być symulowany szybko, w czasie rzeczywistym, skoro świat rzeczywisty działa w czasie rzeczywistym. Z tego powodu kapilary płucne i oskrzela średniego rzędu są traktowane jako elementy o stałych rozłożonych; jednak w taki sposób, że równania różniczkowe opisujące te elementy mogą być rozwiązane ręcznie. W efekcie, nie same równania a ich rozwiązania mogą być wykorzystane w modelu komputerowym.
Tak więc, modele składające się na sztucznego pacjenta są po części modelami o stałych rozłożonych z matematycznego punktu widzenia, ale z punktu widzenia modelu komputerowego są to relatywnie szybko działające modele o stałych skupionych.
Fizjologiczna interpretowalność
Skoro sztuczny/wirtualny pacjent ma być wykorzystywany również przez lekarzy, parametry, które lekarze mogą zmieniać, muszę mieć fizjologiczną lub medyczną interpretację. Dlatego równania powinny mieć taką formę, by ich parametry były interpretowalne, nawet kosztem niepełnej poprawności opisu rzeczywistości. Przykładem może być zależność ciśnienia skoku sprężystego płuc (ciśnienia transpulmonarnego) od objętości płuc: chociaż zazwyczaj zależność tę opisuje się funkcją eksponencjalną, następujący wzór jest wykorzystany w wirtualnym pacjencie:
gdzie:
- Size − parametr, który może być traktowany jako wskaźnik wielkości płuc (‘ilości’ miąższu) w tym znaczeniu, że np. wyższe osoby mają większe płuca a resekcja części płuca zmniejsza wartość tego wskaźnika,
- Compl − parametr, który może być traktowany jako podatność właściwa miąższu (podatność jednostkowej ilości miąższu),
- VA0 − objętość płuc, przy której ciśnienie skoku sprężystego płuc jest równe zeru.
Podział płuc
Wentylacja, perfuzja i wymiana gazowa może być różna w różnych częściach płuc z powodu wpływu grawitacji, niejednorodnych właściwości płuc, ich asymetrycznej pracy, itd. Aby umożliwić symulowanie tych różnic, płuca zostały podzielone na 80 części: zostały podzielone anatomicznie na 5 płatów, a każdy z płatów został podzielony na 16 części trzema płaszczyznami poziomymi (wpływ grawitacji w pozycji stojącej pacjenta) oraz dwiema wzajemnie prostopadłymi płaszczyznami (symulacje pozycji: na wznak i na boku).
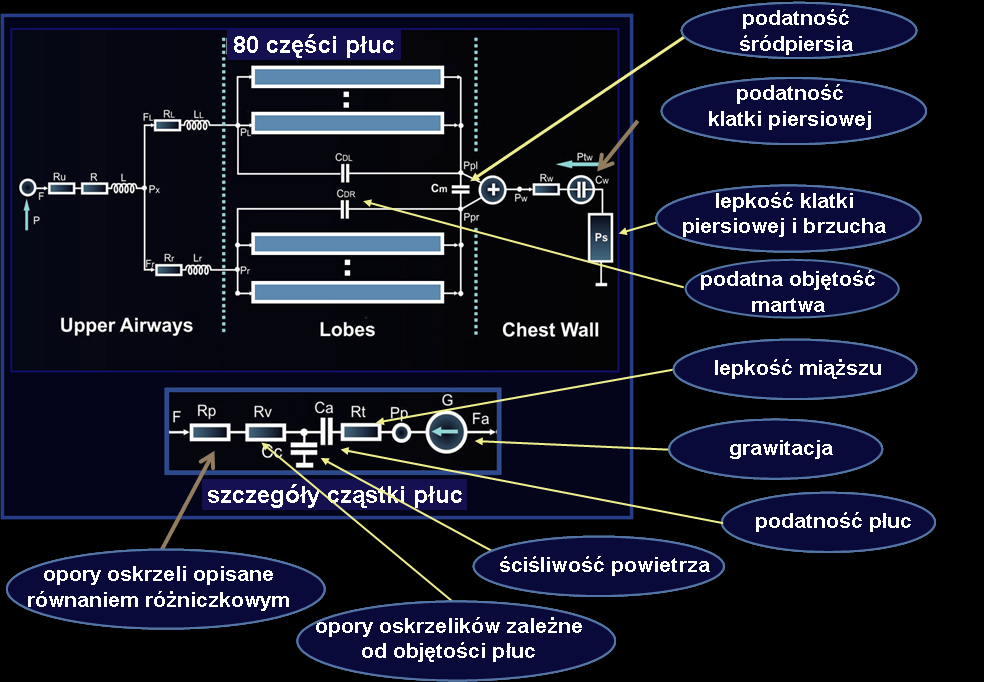
Model mechaniki układu oddechowego
W modelu tym uwzględniono takie pokazane na rysunku elementy anatomiczne i fizjologiczne, które umożliwiają użytkownikowi symulację szerokiej gamy zjawisk, wliczając w to badanie spirometryczne, którego wyniki są całkowicie nieodróżnialne od wyników rzeczywistych pacjentów z takimi samymi chorobami.
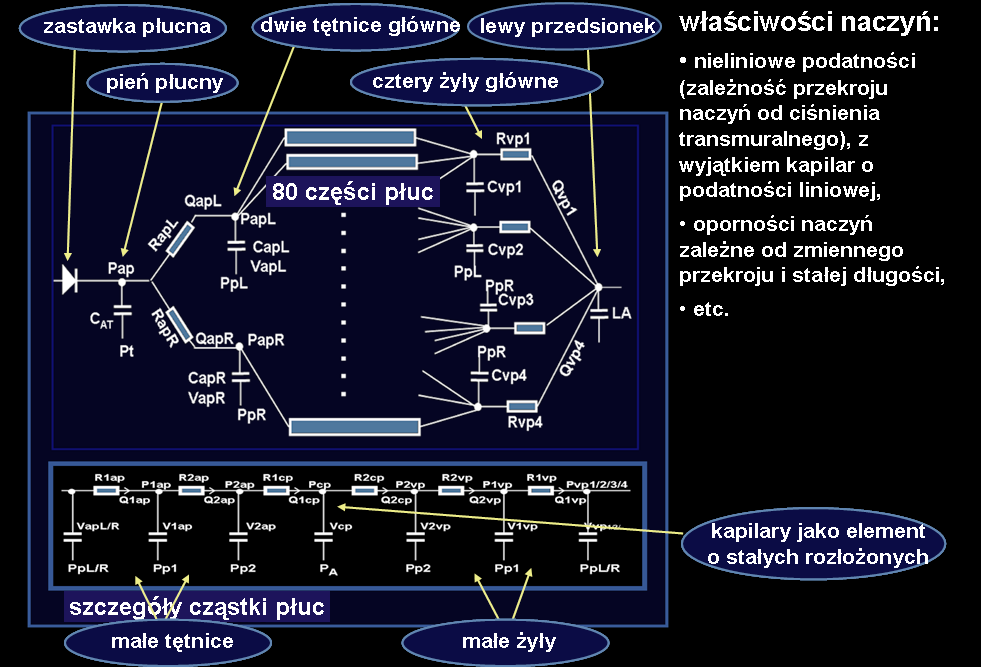
Model krążenia płucnego
W modelu krążenia płucnego przyjęto podział tego krążenia na pień płucny, dwie główne tętnice zaopatrujące prawe i lewe płuco, cztery żyły płucne schodzące się do lewego przedsionka (będącego częścią modelu krążenia systemowego) oraz na następujące unaczynienie każdej z 80 części płuc: kapilara oraz tętnica i żyła – obie podzielone na część proksymalną i dystalną. Kapilara reprezentowana jest przez otrzymane ręcznie rozwiązanie równania różniczkowego, analogicznie jak to ma miejsce w opisanym powyżej przypadku oskrzeli średniego rzędu.
Model wymiany gazowej i transferu gazów
Założono, że możemy mieć do czynienia z powietrzem będącym mieszaniną czterech gazów (tlen, dwutlenek węgla, azot, dodatkowy gaz), których skład procentowy w powietrzu wdychanym jest jednym z parametrów wejściowych białej skrzynki. W przypadku poniższego modułu nr 1, również nasycona para wodna jest uwzględniana.
Model ten składa się z czterech modułów:
- moduł transferu gazów w drogach oddechowych do/z płuc,
- model wymiany gazowej, tj. przechodzenia gazów z/do płuc do/z krwi w kapilarach płucnych; założono, że krew przepływająca przez te kapilary ma dostatecznie dużo czasu, by prężności gazów we krwi końcowo-kapilarnej równe były ciśnieniom parcjalnym tych gazów w pęcherzykach płucnych,
- moduł transportu gazów z krwią w krążeniu płucnym,
- moduł transportu gazów z krwią w krążeniu systemowym, konsumpcji tlenu i produkcji dwutlenku węgla (z uwzględnieniem jednego zastępczego bufora dla CO2).
Trzy pierwsze moduły są integralną częścią wirtualnego pacjenta pneumonologicznego. Czwarty moduł musi być ściśle związany z modelem krążenia systemowego, więc użytkownik, który zechce podłączyć naszego pacjenta do swojego modelu, musi opracować ten moduł samodzielnie (w razie potrzeby służymy pomocą). Należy pamiętać, że różnice w saturacji propagują się wzdłuż naczyń stosunkowo powoli, a więc z punktu widzenia transportu gazów z krwią, naczynia powinny być albo elementami o stałych rozłożonych albo podzielone na szereg segmentów, nawet jeśli z punktu widzenia mechaniki naczynia są pojedynczymi elementami o stałych skupionych. W przypadku modułów 1 i 3 tak właśnie zrobiono, tj. podzielono naczynia i oskrzela na szereg segmentów.
Linki:
Referencje:
- Tgol.e-spirometry system for e-learning of spirometry
- Gólczewski T, Darowski M. Virtual respiratory system and its use in testing of artificial ventilation and ventilatory support methods. Bio-Algorithms and Med-Systems 2005; 1: 65-72 [in Polish]
- Gólczewski T., Darowski M.. Virtual respiratory system for education and research: simulation of expiratory flow limitation for spirometry, Int J Artif Organs 2006; 29: 961–972
- Darowski M, Gólczewski T, Michnikowski M. Choice of proper lung ventilation method. Biocybernetics and Biomedical Engineering, 2006;26(1):21-37
- T. Gólczewski, M. Darowski. Virtual respiratory system in investigation of CPAP influence on optimal breathing frequency in obstructive lungs disease. Nonlinear Biomedical Physic. 2007, 1:6
- T. Gólczewski. Gas exchange in virtual respiratory system — simulation of ventilation without lungs movement. Int J Artif Organs 2007;30:1047-1056
- Gólczewski T, Darowski M. The virtual cardio-respiratory system — a sub-model of gas exchange and transfer.Biocybernetics and Biomedical Engineering. 2008;28(1):29-40
- Gólczewski T, Zieliński K, Ferrari G, Pałko KJ, Darowski M. Influence of Ventilation Mode on Blood Oxygenation – Investigation with Polish Virtual Lungs and Italian Model of Circulation. Biocybern Biomed Eng 2010; 30:17-30
- Golczewski T, Palko KJ. A method for quantification of lung resistive and compliant properties for spirometry interpretation support—Tests on a virtual patient. Biocybern Biomed Eng 2013; 33:136-144

 Polski
Polski English
English